I test di efficacia in vitro permettono di dimostrare dal punto di vista scientifico, le proprietà dal prodotto vantate, con l’obiettivo di supportarne il claim.
Antiossidante
 Al fine di valutare l’azione antiossidante di una materia prima o un prodotto cosmetico/dispositivo medico su colture cellulari viene effettuato il saggio della diclorofluoresceinadiacetato (DCF-DA). Attraverso questo test, viene analizzata la capacità della sostanza di ridurre la formazione dei radicali liberi (riduzione delle ROS) in cellule esposte ad uno stress ossidativo progressivo utilizzando una sonda fluorescente e determinandone l’attività antiossidante.L’attività antiossidante può essere studiata valutando anche l’espressione di attività enzimatiche antiossidanti (SOD, CAT, ect) e il potenziale redox (GSH/GSSG).
Al fine di valutare l’azione antiossidante di una materia prima o un prodotto cosmetico/dispositivo medico su colture cellulari viene effettuato il saggio della diclorofluoresceinadiacetato (DCF-DA). Attraverso questo test, viene analizzata la capacità della sostanza di ridurre la formazione dei radicali liberi (riduzione delle ROS) in cellule esposte ad uno stress ossidativo progressivo utilizzando una sonda fluorescente e determinandone l’attività antiossidante.L’attività antiossidante può essere studiata valutando anche l’espressione di attività enzimatiche antiossidanti (SOD, CAT, ect) e il potenziale redox (GSH/GSSG).
Mercati: Cosmetici, Integratori alimentari, Materie prime.
Claim supportato: Antiossidante, anti-ageing.
Effetto lenitivo
 Tramite questo test viene valutata l’efficacia lenitiva di un prodotto su colture cellulari. In particolare, si valuta l’eventuale tossicità del prodotto tramite il test colorimetrico MTT che permette di stimare la vitalità cellulare e quindi di valutare l’effetto del trattamento con il prodotto da testare. Viene inoltre studiata la variazione nella produzione di specifiche citochine da parte della linea cellulare utilizzata tramite il test ELISA (Enzyme Linked Immunosorbent Assay). Le citochine più studiate sono I’interleuchina 6 (IL-6), l’interleuchina 8 (IL-8) e l’interleuchina IL-1α.
Tramite questo test viene valutata l’efficacia lenitiva di un prodotto su colture cellulari. In particolare, si valuta l’eventuale tossicità del prodotto tramite il test colorimetrico MTT che permette di stimare la vitalità cellulare e quindi di valutare l’effetto del trattamento con il prodotto da testare. Viene inoltre studiata la variazione nella produzione di specifiche citochine da parte della linea cellulare utilizzata tramite il test ELISA (Enzyme Linked Immunosorbent Assay). Le citochine più studiate sono I’interleuchina 6 (IL-6), l’interleuchina 8 (IL-8) e l’interleuchina IL-1α.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Attività lenitiva, Antiinfiammatoria.
Attività anti-pollution
 Al fine di valutare l’azione anti-pollution di un prodotto cosmetico su colture cellulari, viene studiata la riduzione delle specie reattive dell’ossigeno (ROS) in presenza di uno stimolo inquinante. Attraverso questo test, infatti, viene analizzata la capacità di un prodotto o materia prima di proteggere il corpo, in particolare la pelle, dai meccanismi di danno di natura esogena collegati all’inquinamento atmosferico in cellule esposte ad un agente di stress. Nello specifico, per questa tipologia di analisi è stato identificato come stimolo un componente della frazione PM10 del materiale particolato.
Al fine di valutare l’azione anti-pollution di un prodotto cosmetico su colture cellulari, viene studiata la riduzione delle specie reattive dell’ossigeno (ROS) in presenza di uno stimolo inquinante. Attraverso questo test, infatti, viene analizzata la capacità di un prodotto o materia prima di proteggere il corpo, in particolare la pelle, dai meccanismi di danno di natura esogena collegati all’inquinamento atmosferico in cellule esposte ad un agente di stress. Nello specifico, per questa tipologia di analisi è stato identificato come stimolo un componente della frazione PM10 del materiale particolato.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Attività anti-pollution.
Attività detossificante
 La valutazione dell’attività detossificante viene condotta indagando diversi parametri relativi all’eliminazione delle specie reattive dell’ossigeno, ed in particolare:
La valutazione dell’attività detossificante viene condotta indagando diversi parametri relativi all’eliminazione delle specie reattive dell’ossigeno, ed in particolare:
– analisi della produzione di perossido di idrogeno (H2O2), specie reattiva prodotta dalla reazione di riduzione dell’ossigeno cellulare;
– analisi dell’attività dell’enzima Superossido dismutasi (SOD), enzima fondamentale per la dismutazione dell’anione perossido in perossido di idrogeno che successivamente verrà trasformato da altri enzimi in acqua ed ossigeno, come meccanismo di detossificazione;
– analisi della capacità di inibire la formazione dei radicali liberi in cellule esposte ad uno stress ossidativo progressivo mediante analisi in fluorescenza.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Attività detossificante.
Azione smacchiante su denti

L’azione smacchiante viene valutata su denti in resina utilizzati per protesi dentarie. I denti sono pre-trattati con un agente macchiante e in seguito sottoposti ad un trattamento atto a mimare il modo d’uso del prodotto stesso.
I cambiamenti di colore eventualmente dovuti alla possibile azione smacchiante sono valutati visivamente per ottenere parametri qualitativi.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Azione smacchiante.
Protezione del DNA da danno fotoindotto
 Il seguente test si basa su tecniche di biologia cellulare e molecolare per analizzare marcatori di danno del DNA mediante utilizzo di fluorocromi. Le molecole analizzate sono marcatori specifici espressi in seguito a stimolo che danneggia il DNA e indicano la presenza di un eventuale danno del DNA o della fase di riparazione in atto.
Il seguente test si basa su tecniche di biologia cellulare e molecolare per analizzare marcatori di danno del DNA mediante utilizzo di fluorocromi. Le molecole analizzate sono marcatori specifici espressi in seguito a stimolo che danneggia il DNA e indicano la presenza di un eventuale danno del DNA o della fase di riparazione in atto.
Per supportare ulteriormente l’efficacia della sostanza da testare, viene analizzata anche la vitalità cellulare in presenza dello stimolo che induce il danno.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Protezione cutanea da raggi UV.
Effetto protettivo nei confronti del photoageing
 La degradazione del collagene è un segno distintivo dell’invecchiamento della pelle dovuto ai raggi solari o photoageing. In particolare, il collagene di tipo I è la proteina strutturale più abbondante nella matrice extracellulare (ECM) della pelle. L’irradiazione UV provoca alterazioni nel collagene cutaneo attraverso l’inibizione della biosintesi di procollagene di tipo I, con conseguente perdita di contenuto di collagene e aumento della sintesi delle metalloproteinasi, specialmente di tipo I (MMP-1).
La degradazione del collagene è un segno distintivo dell’invecchiamento della pelle dovuto ai raggi solari o photoageing. In particolare, il collagene di tipo I è la proteina strutturale più abbondante nella matrice extracellulare (ECM) della pelle. L’irradiazione UV provoca alterazioni nel collagene cutaneo attraverso l’inibizione della biosintesi di procollagene di tipo I, con conseguente perdita di contenuto di collagene e aumento della sintesi delle metalloproteinasi, specialmente di tipo I (MMP-1).
Con questo scopo, vengono eseguiti saggi immunoenzimatici per studiare i livelli di pro-collagene di tipo I e metalloproteinasi-1 in presenza di irraggiamento per valutare un possibile effetto protettivo, in termini di photo-ageing, del prodotto da testare.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Anti-ageing, Protettivo nei confronti del danno indotto dall’invecchiamento cutaneo.
Rigenerazione di ferite
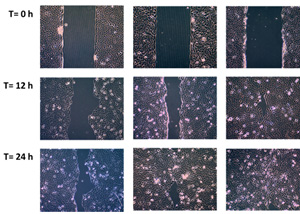 Questo saggio, derivato dalla ricerca biomedica per lo studio della cinetica di riparazione delle ferite, valuta la rigenerazione delle cellule della pelle in seguito a trattamento con una sostanza. Il parametro analizzato consiste nel monitoraggio della motilità cellulare in seguito all’induzione di un taglio nel monostrato cellulare, seguito mediante un time-course fotografico della chiusura del taglio.
Questo saggio, derivato dalla ricerca biomedica per lo studio della cinetica di riparazione delle ferite, valuta la rigenerazione delle cellule della pelle in seguito a trattamento con una sostanza. Il parametro analizzato consiste nel monitoraggio della motilità cellulare in seguito all’induzione di un taglio nel monostrato cellulare, seguito mediante un time-course fotografico della chiusura del taglio.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Effetto rigenerante, Stimolazione della riparazione di ferite.
Stimolazione della sintesi di collagene
 Il collagene è la proteina più abbondante all’interno del nostro corpo e si trova accumulata nella matrice extracellulare (ECM) di tessuti connettivi come la pelle. Con l’aumentare dell’età, si assiste ad un invecchiamento cutaneo con conseguente riduzione della sintesi di collagene. Il saggio di valutazione della sintesi di collagene da noi proposto, permette di valutare la capacità di un prodotto di stimolarne la sintesi in fibroblasti dermici umani, favorendo la minimizzazione delle rughe cutanee.
Il collagene è la proteina più abbondante all’interno del nostro corpo e si trova accumulata nella matrice extracellulare (ECM) di tessuti connettivi come la pelle. Con l’aumentare dell’età, si assiste ad un invecchiamento cutaneo con conseguente riduzione della sintesi di collagene. Il saggio di valutazione della sintesi di collagene da noi proposto, permette di valutare la capacità di un prodotto di stimolarne la sintesi in fibroblasti dermici umani, favorendo la minimizzazione delle rughe cutanee.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Attività anti-ageing.
Stimolazione della sintesi di elastina
 L’elastina è una proteina strutturale, fondamentale per l’elasticità dei tessuti e in particolare della pelle. Con l’aumentare dell’età, si assiste ad un invecchiamento cutaneo con conseguente riduzione dell’elasticità. Il saggio di valutazione della sintesi di elastina, da noi proposto, permette di valutare la capacità di un prodotto di stimolarne la sintesi in fibroblasti dermici umani, favorendo la minimizzazione delle rughe cutanee.
L’elastina è una proteina strutturale, fondamentale per l’elasticità dei tessuti e in particolare della pelle. Con l’aumentare dell’età, si assiste ad un invecchiamento cutaneo con conseguente riduzione dell’elasticità. Il saggio di valutazione della sintesi di elastina, da noi proposto, permette di valutare la capacità di un prodotto di stimolarne la sintesi in fibroblasti dermici umani, favorendo la minimizzazione delle rughe cutanee.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Stimolazione dell’elastina, Attività rigenerante, Attività anti-ageing, Attività anti-rughe.
Effetto idratante
 L’analisi consiste nel valutare l’eventuale stimolazione dell’espressione dei canali cellulari dell’acqua da parte della materia prima/prodotto finito attraverso una metodica che permette di esaminare questo aspetto su cellule integre. Non viene quindi intaccata l’integrità della struttura cellulare e il risultato ottenuto consente di avere un valore effettivo dell’idratazione cellulare su un modello comparabile all’ambiente fisiologico in cui le cellule stesse si trovano nell’organismo.
L’analisi consiste nel valutare l’eventuale stimolazione dell’espressione dei canali cellulari dell’acqua da parte della materia prima/prodotto finito attraverso una metodica che permette di esaminare questo aspetto su cellule integre. Non viene quindi intaccata l’integrità della struttura cellulare e il risultato ottenuto consente di avere un valore effettivo dell’idratazione cellulare su un modello comparabile all’ambiente fisiologico in cui le cellule stesse si trovano nell’organismo.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Effetto idratante, Mantenimento del corretto scambio di acqua tra le cellule della pelle.
Mucoadesività
 Il contatto di sostanze nocive o irritanti con le mucose può determinarne una loro penetrazione provocando gravi effetti degenerativi. Per questo motivo, la creazione di ulteriori barriere sulle mucose, mediante somministrazione di sostanze con proprietà mucoadesive, può contribuire a proteggere le mucose stesse dal rischio di aggressione.Al fine di valutare la mucoadesività di prodotti destinati al trattamento delle mucose, viene effettuata una valutazione della percentuale di inibizione del legame di proteine specifiche mediante metodologia di biologia molecolare.
Il contatto di sostanze nocive o irritanti con le mucose può determinarne una loro penetrazione provocando gravi effetti degenerativi. Per questo motivo, la creazione di ulteriori barriere sulle mucose, mediante somministrazione di sostanze con proprietà mucoadesive, può contribuire a proteggere le mucose stesse dal rischio di aggressione.Al fine di valutare la mucoadesività di prodotti destinati al trattamento delle mucose, viene effettuata una valutazione della percentuale di inibizione del legame di proteine specifiche mediante metodologia di biologia molecolare.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Efficacia della mucoadesione.
Effetto barriera
 Il saggio intende valutare l’effetto barriera esercitato dal prodotto in esame su un supporto di epidermide tridimensionale ricostruita in vitro in grado di mimare l’azione dell’epidermide umana, in presenza di un noto agente irritante.
Il saggio intende valutare l’effetto barriera esercitato dal prodotto in esame su un supporto di epidermide tridimensionale ricostruita in vitro in grado di mimare l’azione dell’epidermide umana, in presenza di un noto agente irritante.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Effetto barriera, Protezione tissutale da agenti dannosi.
Analisi dell'adipogenesi
 Mediante il seguente saggio viene studiata l’inibizione dell’adipogenesi, ovvero della sintesi di nuovi depositi di acidi grassi, indotta da una sostanza in colture cellulari di adipociti differenziati tramite colorazione e successiva quantificazione dei lipidi accumulati all’interno delle cellule.
Mediante il seguente saggio viene studiata l’inibizione dell’adipogenesi, ovvero della sintesi di nuovi depositi di acidi grassi, indotta da una sostanza in colture cellulari di adipociti differenziati tramite colorazione e successiva quantificazione dei lipidi accumulati all’interno delle cellule.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Inibizione dell’adipogenesi.
Analisi della lipolisi
 La lipolisi è il processo mediante il quale i trigliceridi sono idrolizzati in glicerolo e acidi grassi che vengono rilasciati nel circolo sanguigno, mediante il quale possono raggiungere altri tessuti e produrre altri effetti, come ad esempio la formazione della cellulite.
La lipolisi è il processo mediante il quale i trigliceridi sono idrolizzati in glicerolo e acidi grassi che vengono rilasciati nel circolo sanguigno, mediante il quale possono raggiungere altri tessuti e produrre altri effetti, come ad esempio la formazione della cellulite.
Il metodo analitico prevede il dosaggio del glicerolo rilasciato da colture cellulari di adipocidi differenziati in seguito a trattamento con la sostanza da testare, valutando quindi l’eventuale capacità di quest’ultima di modulare la reazione lipolitica.
Mercati: Cosmetici, Dispositivi medici, Materie prime.
Claim supportato: Analisi della lipolisi.
